Sistema Immunitario e 5LB
08 maggio 2020
La salute sta tanto al di sopra di tutti i beni esteriori,
che in verità un mendico sano è più felice di un re malato.
Arthur Schopenhauer
Il sistema immunitario è sostanzialmente una rete di componenti cellulari e solubili che interagiscono tra loro. La sua funzione è quella di distinguere ciò che appartiene all'organismo (self) da ciò che non gli appartiene (non-self), provvedendo ad eliminare tutto ciò che non appartiene al corpo. Occorre però considerare che ciò che fa parte dell'organismo di un individuo, può estendersi oltre le barriere di questo organismo. Ad esempio un individuo può considerare parte del proprio organismo i microbi che sono presenti nel suo ambiente, ma se in questo ambiente viene introdotto un nuovo microorganismo, il corpo di quell'individuo potrebbe non riconoscerlo. Si affaccia quindi il concetto per il quale il sistema immunitario è totalmente influenzato dal vissuto della persona e dalle sue percezione psico-biologiche.
Riconosciamo, nel sistema immunitario, due meccanismi: le difese naturali aspecifiche e l'immunità vera e propria, le quali sono legate una all'altra e si influenzano reciprocamente.
1. Difese naturali aspecifiche (innate)
È presente fin dalla nascita, non necessita di un precedente contatto con la sostanza estranea e non crea memoria immunitaria. Comprendono le barriere meccaniche, come la cute e le sierose interne (mesoderma laterale), e le barriere chimiche, come il succo acido gastrico.
In questo tipo di difesa esistono due componenti cellulari:
- il sistema fagocitario, la cui funzione è quella di ingerire e digerire i microrganismi invasori
- le cellule natural killer (NK), la cui funzione è quella di eliminare alcuni tipi di tumori, di microrganismi e di cellule infettate da virus.
Le componenti solubili sono costituite dalle proteine del complemento, dai reattanti di fase acuta e dalle citochine.
I fagociti includono i neutrofili e i monociti (nel sangue) e i macrofagi (nei tessuti).
Ampiamente distribuiti, i macrofagi sono localizzati in maniera strategica nei punti in cui i tessuti sono a contatto con il sangue o con gli spazi cavitari; ne sono esempi i macrofagi alveolari (nei polmoni), le cellule di Kupffer (nei sinusoidi epatici), le cellule sinoviali (nelle cavità articolari), le cellule microgliali perivascolari (a protezione del SNC), i fagociti mesangiali (nei reni).
Le citochine sono polipeptidi non immunoglobulinici secreti dai monociti e dai linfociti in risposta alla loro interazione con un Antigene specifico, con un antigene aspecifico, oppure in risposta a uno stimolo aspecifico solubile (es. endotossine, altre citochine). Le citochine modulano l'ampiezza delle risposte infiammatorie o immunitarie. Sebbene la loro secrezione possa essere indotta dall'interazione di un linfocita con il suo antigene specifico, le citochine non sono antigene-specifiche; pertanto esse costituiscono un tramite tra l'immunità innata e quella adattativa.
2. Immunità specifica (adattativa)
Le caratteristiche distintive dell'immunità adattativa sono la capacità di apprendimento, l'adattabilità e la memoria.
La sua componente cellulare è costituita dai linfociti, mentre le immunoglobuline ne rappresentano la componente solubile.
I linfociti sono divisi in due sottopopolazioni:
- quelli derivati dal timo (cellule T)
- quelli derivati dal midollo osseo (cellule B).
I linfociti sono ripartiti in cloni e ogni clone si specializza nel riconoscimento di un antigene specifico per mezzo del suo recettore per l'antigene. Il complesso problema di dover provvedere a un numero infinito di cloni altamente specifici, viene risolto grazie alla capacità dei geni, per il recettore antigenico dei linfociti, di riarrangiarsi in una serie di combinazioni pressoché illimitate.
La funzione di recettore per l'antigene sulla membrana delle cellule B è svolta dalle immunoglobuline di superficie (sIg).
Dopo che le cellule B hanno legato un antigene solubile per mezzo delle loro sIg, una serie di eventi cellulari (es. proliferazione, differenziazione) porta alla secrezione di una immunoglobulina che costituisce l'anticorpo (Ac) specifico per quell'antigene.
L'opinione attuale (quindi non provata) è che il corredo anticorpale che un organismo possiede prima di venire in contatto con gli antigeni, sia costituito da anticorpi prodotti durante la maturazione delle cellule B attraverso riarrangiamenti dei geni per le Ig.
Per capire la natura dell'organizzazione dei geni per le immunoglobuline è necessario comprendere la struttura delle immunoglobuline.
Le immunoglobuline sono composte di due catene pesanti e due catene leggere, ognuna con regioni costanti (C) e regioni variabili (V). L'antigene viene legato in corrispondenza della regione variabile.
Cellule T
Le cellule T non possiedono sIg, ma riconoscono gli antigeni attraverso il loro strumento di riconoscimento principale, il recettore delle cellule T (T-Cell Receptor, TCR) e altre molecole di adesione accessorie. I geni che codificano per il TCR appartengono alla superfamiglia dei geni delle immunoglobuline; analogamente ai geni per le immunoglobuline, essi vanno incontro a ricombinazione, dando luogo così a un gran numero di cloni di cellule T, ciascuno dotato di una responsività antigenica specifica.
I linfociti possono essere ulteriormente suddivisi in sottopopolazioni a seconda della funzione che svolgono o dei loro marker di superficie. Le sottopopolazioni linfocitarie sono state identificate grazie alle diverse combinazioni di determinate molecole presenti sulla loro membrana: questi marker di superficie sono stati denominati Cluster di Differenziazione (CD). Fino a oggi, sono stati identificati 166 CD.
Citochine
Sebbene sia necessario un intimo contatto cellulare perché le risposte T-cellulari siano ottimali, le cellule T e i monociti secernono citochine, le quali sono in grado di influenzare eventi biologici che avvengono localmente o a distanza. Esse interagiscono con specifici recettori della superficie cellulare e possono agire in maniera autocrina (sistema di segnalazione cellulare in cui una sostanza - agente autocrino - prodotta da una cellula va a modificare il comportamento della cellula stessa) o paracrina (il messaggero chimico prodotto da una cellula che, diffondendosi, modifica la fisiologia delle cellule che la circondano).
Le citochine possono essere divise in diversi gruppi, i quali comprendono gli Interferoni (IFN-a, b e g), il Tumor Necrosis Factor (TNF-a e b), le Interleuchine (dall'IL-1 all'IL-18), i Transforming Growth Factor e i Colony Stimulating Factor (CSF) emopoietici.
Anche se le diverse citochine e i loro effetti vengono di solito elencati separatamente, è importante ricordare che in una determinata risposta immunitaria le citochine agiscono di concerto, in coppia, oppure in conflitto tra loro. Per esempio l'IL-1 induce la secrezione di IL-2; l'IL-2, l'IL-4 e l'IL-6 possono agire sinergicamente nella generazione dei linfociti T citotossici; l'IL-4 e l'IFN-g possono neutralizzare l'uno gli effetti dell'altro nell'induzione dell'espressione degli antigene di classe II sulle cellule B e nell'induzione della secrezione di IgE.
Una nuova famiglia di citochine è quella che è stata appropriatamente denominata delle chemiochine; esse inducono la chemiotassi e la migrazione delle sottopopolazioni dei leucociti. Esistono quattro sottotipi di chemiochine, i quali sono definiti in base al numero di aminoacidi interposti tra i primi due residui di cisteina della molecola. Alcuni dei recettori per le chemiochine potrebbero servire come corecettori per l'ingresso del HIV all'interno dei monociti/macrofagi.
| Citochine | Produzione | Effetti principali |
|---|---|---|
| Interleuchine (IL) | ||
| IL-1α, IL-1β | Monociti, macrofagi | Febbre, sonno, anoressia, infiammazione, attivazione dei linfociti, produzione di IL-6 e CSF |
| IL-2 | Cellule T | Induzione della crescita delle cellule T, costimolazione della crescita e della differenziazione delle cellule B, aumento delle NK e delle LAK |
| IL-3 | Cellule T, mast-cellule [1] | Induzione della crescita delle mast-cellule, crescita delle cellule emopoietiche pluripotenti |
| IL-4 | cellule T, mast-cellule | Induzione della crescita delle cellule T e della generazione dei CTL, costimolazione della crescita delle cellule B, sinergismo con l'IL-3 nella crescita delle mast-cellule, della produzione di IgE e IgG4, induzione dell'espressione e del rilascio del CD23, del MHC di classe II sulle cellule B, switch da TH a TH2 |
| IL-5 | cellule T, mast-cellule | Induzione della differenziazione degli eosinofili, della produzione di IgA, costimolazione della crescita delle cellule B |
| IL-6 | Monociti, fibroblasti, cellule T | Pirogeno, induzione della crescita dei plasmocitomi e degli ibridomi, amplificazione della produzione di Ig, del MHC di classe I sui fibroblasti, sinergismo con l'IL-2 nella produzione delle proteine di fase acuta da parte degli epatociti, sinergismo con l'IL-3 nella crescita delle celluleemopoietiche, induzione della differenziazione dei CT |
| IL-7 | Cellule stromali del midollo osseo e del timo | Induzione della proliferazione delle cellule pro-B e pre-B e dei timociti immaturi |
| IL-8 (chemiochina) | Monociti, cellule endoteliali, macrofagi alveolari, fibroblasti | Induzione della chemiotassi e dell'attivazione dei neutrofili e delle cellule T |
| IL-9 | cellule T | Induzione della proliferazione di alcune cellule T, potenziamento della crescita delle mast-cellule indotta dall'IL-3 |
| IL-10 | cellule T, cellule B attivate, monociti | ↓ del MHC di classe II, inibizione dell'attivazione del MAC, ↓ della presentazione dell'antigene, stimolazione della proliferazione delle cellule B e della produzione di Ac, stimolazione delle mast-cellule, switch da THa TH2 |
| IL-11 | Cellule del microambiente emopoietico | Stimolazione della produzione di Ac, sinergismo con l'IL-3 nella proliferazione dei megacariociti, stimolazione dei precursori dei macrofagi |
| IL-12 | Monociti, macrofagi, alcune cellule B, alcune mast- cellule | Attivazione della secrezione di IFN-g da parte delle NK, switch da TH a TH1, inibizione della secrezione di IgE indotta dall'IL-4 |
| IL-13 | cellule B, macrofagi | Induzione della secrezione di IgE |
| IL-14 | cellule T | Induzione del fattore di crescita delle cellule B |
| IL-15 | Cellule non linfoidi, muscolo | Induzione della crescita e della citotossicità delle cellule NK, differenziazione delle cellule NK |
| IL-16 | cellule T (preformata nei CD8) | Chemiotassi dei CD4, induzione del CD25, del MHC di classe II, repressione della trascrizione dell'HIV |
| IL-17 | Cellule CD4 di memoria | Costimolazione della proliferazione delle cellule T, in duzione della secrezione di IL-6, IL-8 e G-CSF da parte delle cellule epiteliali, endoteliali e fibroblastiche |
| Interferoni (IFN) | ||
| IFN-α | Leucociti | Inibizione della replicazione virale e della crescita tumorale, dell'espressione del MHC di classe I e di classe II, dell'attività NK, modulazione della risposta Ac |
| IFN-β | Fibroblasti | Stesse attività dell'IFN-a |
| IFN-γ | cellule T, NK | attivazione dei macrofagi, dell'attività NK, ↓ della secrezione di CD23 e di IgE indotta dall'IL-4, costimolazione della crescita e della differenziazione delle cellule B |
| Tumor necrosis factor (TNF) | ||
| TNF-α(cachessina) | Monociti, macrofagi | Induzione dell'IL-1, delle molecole di adesione e del MHC di classe I sulle cellule endoteliali, pirogeno, in duzione del GM-CSF, effetto citotossico/citostatico, induzione della secrezione di IFN-γ |
| TNF-β | cellule T | Fattore citotossico |
| Colony-stimulating factor (CSF) | ||
| GM-CSF | cellule T, macrofagi, monociti, cellule endoteliali | Induzione della crescita dei precursori dei granulociti e dei monociti, attivazione dei macrofagi, della produzione di leucotrieni da parte degli eosinofili, dell'attività tumoricida dei monociti |
| G-CSF | Monociti, fibroblasti, cellule endoteliali | Induzione della crescita dei granulociti |
| M-CSF | Monociti, fibroblasti, cellule endoteliali | Induzione della crescita dei monociti |
| Transforming growth factor (TGF) | ||
| TGF-α | Tumori solidi (carcinomi >sarcomi), monociti | Induzione dell'angiogenesi, proliferazione dei cheratinociti, riassorbimento osseo, crescita tumorale |
| TGF-β | Piastrine, placenta, rene, osso, cellule T e B | Induzione della proliferazione dei fibroblasti; sintesi del collagene e della fibronectina; inibizione dei CTL, delle NK e delle LAK; inibizione della proliferazione delle cellule T e B; potenziamento della guarigione delle ferite e dell'angiogenesi |
| Chemiochine | ||
| C. Esempio: linfotassina (LPTN) | CD8 attivati, NK, mast-cellule | Induzione della chemiotassi delle cellule T e delle cellule NK |
| C-C | Variabile | Induzione della chemiotassi delle cellule T, delle cellule NK, dei basofili e degli eosinofili |
| C-X-C | Variabile | Induzione della chemiotassi delle cellule T, delle mast-cellule, dei monociti e degli eosinofili |
| C-X3-C | Variabile | Ancora non ben caratterizzati |
| mast-cellule = genesi delle reazioni allergiche, di ipersensibilità e anafilattiche, attivatori della flogosi acuta. ↓=diminuzione; Ac=anticorpi; CSF=colony-stimulating factor; CTL=linfociti T citotossici; G=granulociti; GM=granulociti/macrofagi; LAK=cellule killer attivate dalle linfochine; MAC=complesso di attacco alla membrana; MHC=complesso maggiore di istocompatibilità; NK=cellule natural killer; TH=T helper. | ||
Cellule B e immunità umorale
Le cellule B costituiscono dal 5 al 15% dei linfociti del sangue e sono morfologicamente indistinguibili dalle cellule T. Tuttavia, esse possono essere riconosciute fenotipicamente per la presenza di sIg e per la presenza del CD19, CD20, CD21 (CR2), CD49c, CD72 e CD80. Inoltre le cellule B possono esprimere il MHC di classe II e una varietà di altri CD che non sono loro specifici. All'interno dei linfonodi, le cellule B si trovano nella zona corticale sottocapsulare esterna; nella milza, esse sono contenute nella zona marginale e nei follicoli.
Le cellule B sembrano svilupparsi secondo una serie di fasi programmate. Queste tappe hanno inizio nel midollo osseo con la cellula staminale orientata, proseguono attraverso gli stadi di cellula pro-B precoce e tardiva e lo stadio di cellula pre-B, e si concludono con la cellula B immatura. Non sembra che l'antigene abbia un ruolo nell'indirizzare questa sequenza, ma l'interazione delle cellule B immature con l'antigene può condurre all'inattivazione clonale o alla tolleranza. Le cellule B immature che non vengono inattivate possono continuare a svilupparsi fino a diventare cellule B mature antigenicamente vergini e lasciare il midollo per colonizzare gli organi linfoidi periferici. In essi, l'interazione tra sIgG e antigeni estranei le trasforma in linfoblasti. Giunte al termine della loro differenziazione, queste cellule B diventano plasmacellule, le quali secernono immunoglobuline di una sola classe.
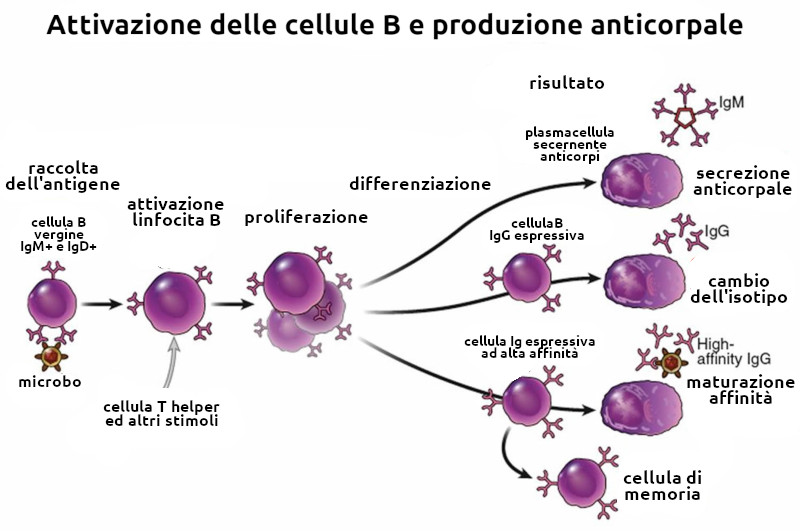
Le cellule B presenti nei tessuti periferici sono preorientate a rispondere a un limitato numero di antigeni. La prima interazione tra la cellula B e l'antigene è conosciuta come risposta immunitaria primaria e le cellule B orientate a rispondere a questo antigene vanno incontro a differenziazione e proliferazione clonale. Alcune divengono cellule di memoria; altre si differenziano in plasmacellule mature sintetizzanti anticorpi.
Le caratteristiche principali della risposta immunitaria primaria sono la presenza di un periodo di latenza prima della comparsa degli anticorpi, la produzione soltanto di una piccola quantità di anticorpi, inizialmente IgM e successivamente uno switch dell'isotipo delle immunoglobuline (con la collaborazione delle cellule T) verso le IgG, le IgA o le IgE. Ciò porta alla generazione di un gran numero di cellule di memoria in grado di rispondere in futuro al medesimo antigene.
La risposta immunitaria secondaria (anamnestica o amplificata) ha luogo in occasione dei successivi contatti con lo stesso antigene. Le sue caratteristiche principali sono la rapida proliferazione delle cellule B, la rapida differenziazione in plasmacellule mature e la sollecita produzione di grandi quantità di anticorpi, soprattutto IgG, che vengono liberati nel sangue e in altri tessuti dell'organismo dove possono venire a contatto con l'antigene in condizioni ottimali e reagire efficacemente con esso. In risposta al medesimo antigene possono essere prodotte IgM, IgG e IgA. Così le cellule B derivate da una singola cellula B matura, antigenicamente vergine, possono differenziarsi in una famiglia di cellule B geneticamente programmate per sintetizzare anticorpi aventi una singola specificità antigenica, con cloni rappresentativi orientati alla produzione di ciascuna delle classi delle immunoglobuline (ad esempio IgM, IgG, IgA).
3. Antigeni e anticorpi
Struttura degli antigeni e antigenicità
Un antigene è una sostanza in grado di evocare risposte immunitarie specifiche. Una volta prodotti, gli anticorpi sono quindi in grado di combinarsi con antigeni specifici, più o meno come i pezzi di un puzzle. Gli anticorpi riconoscono i siti di combinazione degli antigeni, i quali consistono in configurazioni steriche specifiche (epitopi o determinanti antigenici) sulle superfici di grandi molecole ad alto peso molecolare (ad esempio proteine, polisaccaridi e acidi nucleici). La presenza di un epitopo di questo genere rende una molecola un antigene.
I siti di combinazione dell'anticorpo e dell'antigene si incastrano saldamente tra loro con una potente forza attrattiva, perché le aree di appaiamento sulla superficie di ciascuna molecola sono relativamente ampie. La stessa molecola anticorpale può inoltre reagire in maniera crociata con antigeni tra loro correlati, se i determinanti sulla loro superficie sono sufficientemente simili a quelli presenti sull'antigene originale. Le sostanze sono immunogene (antigeniche) se il sistema immunitario è in grado di riconoscerne i determinanti antigenici come estranei (non-self) e se il peso molecolare della sostanza è sufficientemente elevato. (il che permette di capire come mai il sistema immunitario non riconosca le cellule tumorali come qualcosa di non-self, perché di fatto sono un prodotto del corpo da non contrastare)
Struttura degli anticorpi
Le molecole anticorpali sono immunoglobuline che possiedono sequenza aminoacidica e una struttura terziaria particolari, che conferiscono loro la capacità di legarsi a una struttura complementare situata sull'antigene. Nonostante tutte le immunoglobuline siano probabilmente anticorpi, non è sempre possibile conoscere l'antigene contro il quale ciascuna immunoglobulina è diretta. La reazione antigene-anticorpo può svolgere un ruolo specifico nella protezione dell'ospite contro virus, batteri e altri patogeni.
Le molecole anticorpali sono estremamente eterogenee e nel loro complesso sono in grado di combinarsi con un numero di antigeni praticamente illimitato, tuttavia condividono alcune caratteristiche comuni.
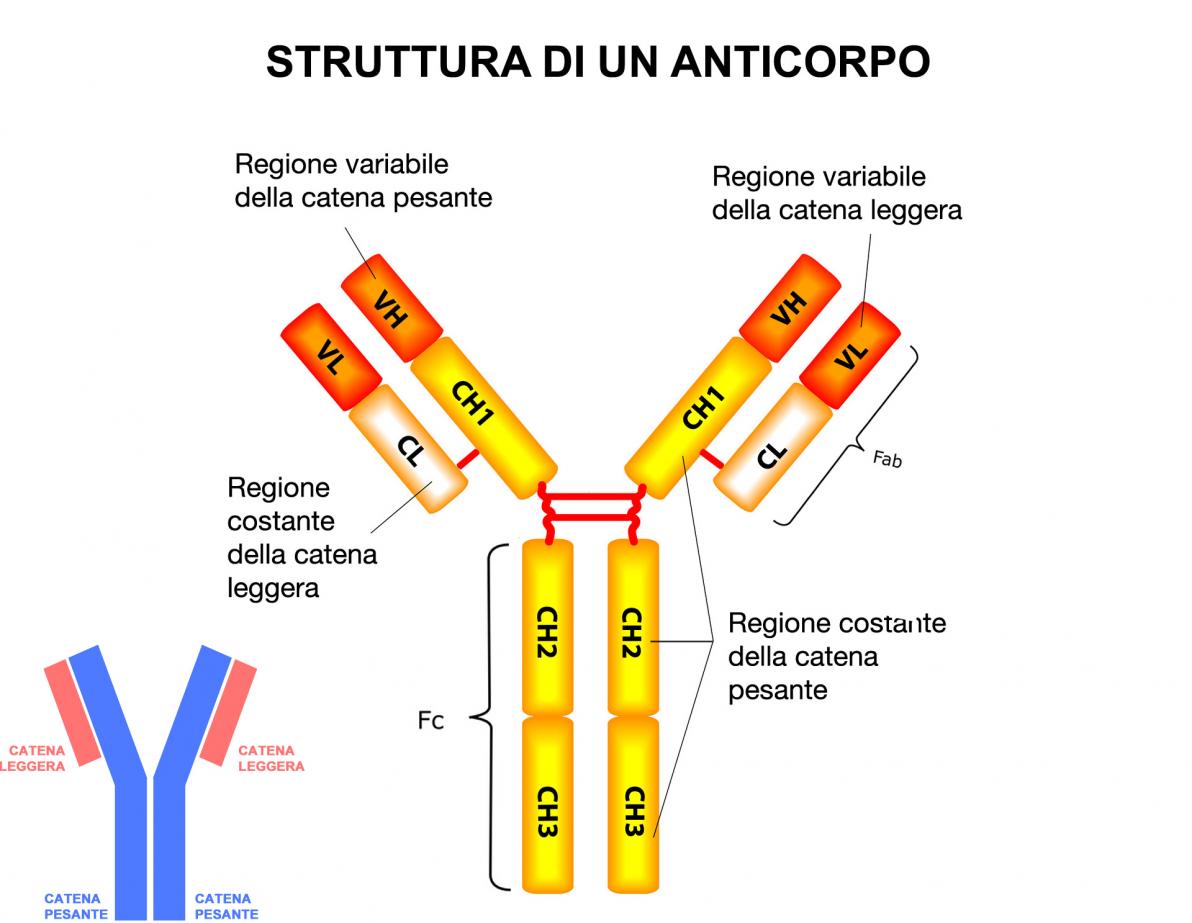
La molecola immunoglobulina a forma di Y si compone di una regione variabile (V) e di una regione costante (C).
La regione V è situata alle estremità distali delle braccia della Y ed è chiamata così a causa dell'alta variabilità degli aminoacidi che vi si trovano, i quali determinano di volta in volta la capacità dell'immunoglobulina di combinarsi con l'antigene. La regione C, prossimale al sito di combinazione con l'antigene, contiene una sequenza aminoacidica relativamente costante la quale è caratteristica di ciascuna classe di immunoglobuline.
Proprietà biologiche degli anticorpi
La struttura aminoacidica della regione C della catena pesante determina l'isotipo della classe di immunoglobulina cui appartiene. Ogni classe svolge funzioni differenti.
È una cascata enzimatica che partecipa al processo di difesa contro le infezioni. Molte proteine del complemento sono presenti nel siero come precursori enzimatici inattivi; altre si trovano sulla superficie delle cellule. Il sistema del complemento collega l'immunità innata e quella acquisita tramite i seguenti meccanismi: - Aumentando le risposte anticorpali e la memoria immunologica - Decomponendo le cellule estranee - Bonificando il microambiente da immunocomplessi e da cellule morte I componenti del complemento hanno numerose funzioni biologiche (stimolazione della chemiotassi, l'induzione dei mastociti IgE-indipendenti alla degranulazione).
- Le IgM
- I primi anticorpi che vengono sintetizzati in seguito a immunizzazione primaria (esposizione a un nuovo antigene), proteggono dalle aggressioni il compartimento intravascolare. Le molecole delle IgM collaborano con il sistema fagocitario nell'eliminazione di molti tipi di microrganismi. Le isoemoagglutinine e molti anticorpi diretti contro i microrganismi Gram- sono IgM. Le IgM monomeriche svolgono la funzione di recettori per l'anticorpo sulla membrana delle cellule B. Le IgG, la classe di anticorpi sierici di gran lunga predominante, si possono trovare anche nei compartimenti extravascolari; vengono prodotte quando il titolo delle IgM comincia a decrescere dopo l'immunizzazione primaria.
- Le IgG
- Sono le principali immunoglobuline prodotte in seguito a reimmunizzazione (risposta immunitaria di memoria o secondaria). Esse proteggono i tessuti dai batteri, dai virus e dalle tossine. Le IgG sono le uniche immunoglobuline in grado di attraversare la barriera placentare. Sottoclassi differenti di IgG neutralizzano le tossine batteriche, attivano il complemento e potenziano la fagocitosi. Le gamma-globuline disponibili in commercio sono costituite quasi interamente da IgG, con piccole quote di altre Ig.
- Le IgA
- Si trovano nelle secrezioni mucose (saliva, lacrime, secrezioni respiratorie, gastro-intestinale GI e genito-urinarie GU, oltre al colostro), dove provvedono a una difesa antibatterica e antivirale di primo livello. Le IgA secretorie vengono sintetizzate nelle regioni subepiteliali dell'apparato GI e di quello respiratorio e sono combinate con una componente secretoria (SeC) prodotta localmente. Alcune cellule produttrici di IgA si trovano nei linfonodi e nella milza.
- Le IgD
- Sono presenti nel siero in concentrazioni estremamente basse, ma compaiono anche sulla superficie delle cellule B in via di maturazione e potrebbero svolgere un ruolo importante nella loro crescita e nel loro sviluppo. Le IgE (anticorpi reaginici, sensibilizzanti cutanei o anafilattici), come le IgA, si trovano principalmente nelle secrezioni mucose respiratorie e GI. Nel siero, sono presenti in concentrazioni molto basse.
- Le IgE
- Interagiscono con le mast-cellule; il legame simultaneo di due molecole di IgE da parte di un allergene può provocare la degranulazione delle cellule, con il rilascio di mediatori chimici che causano una risposta di tipo allergico. I livelli sierici delle IgE sono elevati nelle malattie atopiche (asma allergico o estrinseco, febbre da fieno e dermatite atopica), nelle malattie parassitarie, nel morbo di Hodgkin in fase molto avanzata e nel mieloma monoclonale a IgE. Le IgE possono svolgere un ruolo positivo nella difesa contro i parassiti.
4. Cellule T e Immunità cellulare
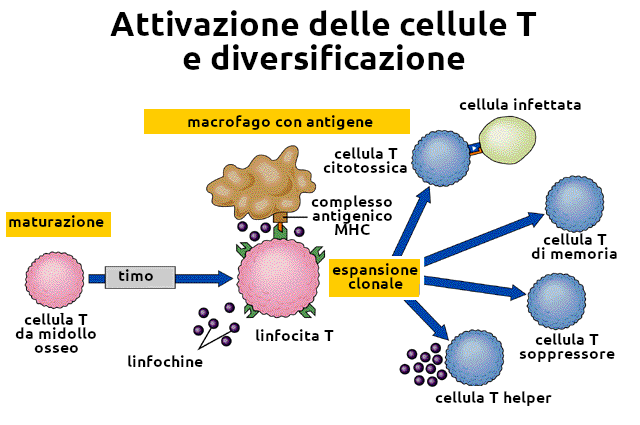
Le cellule T maturano, acquistano capacità funzionali e apprendono il concetto di self all'interno del timo. Il timo svolge il duplice compito della selezione positiva (i cloni che riconoscono il complesso MHC/antigene vengono posti in condizione di proliferare, maturare e migrare in periferia) e della selezione negativa (i cloni che reagiscono al self, riconoscendolo come estraneo, vengono eliminati). Gli esatti meccanismi cellulari e molecolari di questa selezione non sono del tutto conosciuti.
Durante lo sviluppo fetale la cellula staminale T, derivata dal midollo osseo, si sposta nel timo, dove matura e apprende il concetto di self. Si svolge quindi il processo della selezione timica e ai linfociti maturi viene consentito di lasciare la ghiandola; essi si ritrovano nel sangue periferico e all'interno dei tessuti linfoidi. Tutte le cellule T mature esprimono il CD4 o il CD8 in maniera mutuamente esclusiva.
Cellule T helper (TH)
Le cellule T che esprimono il CD4 vengono genericamente denominate linfociti T helper (TH). Queste cellule possono essere suddivise in due categorie principali, a seconda della loro funzione, della risposta a diverse citochine e della capacità di secernere citochine. L'opinione attuale è che le cellule TH siano in origine precursori cellulari sintetizzanti IL-2. In seguito alla stimolazione iniziale, queste cellule si trasformano in cellule TH0, le quali hanno la capacità di secernere diverse citochine, compresi l'IFN-g, l'IL-2, l'IL-4, l'IL-5 e l'IL-10. A seconda della citochina disponibile, le cellule TH0 possono trasformarsi in cellule TH1 oppure in cellule TH2; l'IFN-g e l'IL-12 promuovono lo sviluppo delle TH1 e l'IL-4 e l'IL-10 quello delle TH2. I linfociti TH1 e TH2 differiscono tra loro per il profilo delle citochine che secernono.
In generale, i linfociti TH1 favoriscono l'attivazione dell'immunità cellulare, mentre i linfociti TH2 favoriscono quella dell'immunità umorale. L'identificazione delle risposte TH1 e TH2 ha modificato il modo di considerare le relazioni tra il sistema immunitario e le malattie. Una risposta immunitaria deve essere non solo energica, ma anche appropriata all'infezione o alla malattia. In aggiunta, una risposta TH1 può aggravare le patologie autoimmuni, mentre una risposta TH2 favorisce la secrezione di IgE e lo sviluppo di atopia.
Cellule T suppressor/citotossiche
Le cellule T che esprimono il CD8 sono meno ben caratterizzate rispetto ai sottotipi TH, nonostante sembri che anch'esse possano essere suddivise in due sottotipi sulla base delle citochine che secernono, con criterio identico a quello dei sottotipi dei CD4.
Cellule killer
L'identificazione di ciascun tipo di cellula killer (tra i diversi possibili) dipende dalla restrizione MHC, dalla necessità di sensibilizzazione, dal tipo di bersaglio e dalla risposta alle citochine. Sebbene i macrofagi possano essere citotossici, tale tossicità è aspecifica ed è il risultato della loro attivazione da parte di alcune citochine. I vari tipi di cellule killer possono essere fondamentalmente divisi in cellule con restrizione MHC e cellule senza restrizione MHC (come le cellule NaturalKiller). Nessuno dei due tipi richiede anticorpi, complemento o fagocitosi per eliminare le cellule bersaglio; al contrario, esse trasmettono il segnale litico attraverso la membrana della cellula bersaglio dopo aver stabilito con essa un intimo contatto intercellulare.
5. Reti immunitarie
Il sistema immunitario si comporta come un'unità indivisibile e nessuna delle sue componenti agisce in maniera autonoma. In ogni risposta immunitaria, le varie componenti agiscono di concerto, in tandem o in conflitto tra loro, come è esemplificato dalla capacità del sistema immunitario di eliminare i microrganismi. I microrganismi extracellulari (la maggior parte dei batteri capsulati) per essere digeriti devono solo essere fagocitati; al contrario i microrganismi intracellulari (es. i micobatteri) vengono facilmente ingeriti, ma non possono essere digeriti a meno che il macrofago non riceva un segnale di attivazione. La strategia per eliminare i microrganismi extracellulari è pertanto orientata alla fagocitosi, la quale viene facilitata dall'opsonizzazione (rivestimento di un microrganismo con anticorpi e/o con prodotti del complemento). Poiché la maggior parte dei fagociti possiede recettori per la porzione Fc degli anticorpi e per i prodotti del C3, la presenza di queste molecole su un batterio facilita la sua adesione e la sua ingestione. Questa risposta immunitaria "semplice" dipende dal buon esito della sintesi di anticorpi, dall'attivazione della cascata complementare e dall'integrità del sistema fagocitario. Gli anticorpi vengono prodotti dalle cellule B, tuttavia queste cellule sono soggette all'azione di induzione o di soppressione da parte delle cellule T.
In aggiunta, i fagociti vengono richiamati da fattori chemiotattici, alcuni dei quali sono sintetizzati dalle cellule T. La strategia per eliminare alcuni microrganismi intracellulari che infettano i fagociti prevede l'attivazione delle cellule ospiti, le quali successivamente divengono "armate" e capaci di uccidere questi organismi in maniera aspecifica. La capacità di attivare i macrofagi costituisce il nucleo fondamentale della tipica reazione di ipersensibilità ritardata (DTH) e il test cutaneo di DTH è un esempio eccellente delle diverse cascate di eventi coinvolte in una determinata risposta immunitaria. Il presupposto di un test cutaneo di DTH è che l'iniezione intradermica di un antigene con il quale il paziente sia venuto a contatto in precedenza conduca all'indurimento cutaneo locale entro 48 h.
6. Secondo le 5 Leggi Biologiche
Il Sistema Immunologico è un insieme di organi e meccanismi incaricati di riconoscere gli agenti nocivi e distruggerli. La sua missione è quella di proteggere l'organismo.
- Foglietto embrionale: Mesoderma dorsale o recente.
- Senso biologico: Difendere l'organismo dagli agenti patogeni, dagli invasori esterni.
- Conflitto: Conflitti di inadeguatezza e svalutazione relativi a temi di attacco e difesa. Un abbassamento del sistema immunitario indica una mancata autorizzazione a difendersi, sia in fase attiva che in fase di riparazione. "Per poter sopravvivere non devo difendermi, non devo rispondere.
Il Timo è un organo ghiandolare endocrino molto attivo durante l'infanzia. È la ghiandola principale del sistema immunitario e la sua funzione è quella di sviluppare e maturare i linfociti T.
- Foglietto embrionale: Mesoderma dorsale o recente.
- Senso biologico: Difesa dell'organismo attraverso i linfociti T. Ha una importante funzione nella crescita e nell'adattamento del sistema immunitario.
- Conflitto: Conflitto di difesa nel contesto della famiglia. Ci portano via le cose più essenziali nella nostra esistenza.
Conflitto di negazione alla crescita. Bisogno costante della protezione materna per poter sopravvivere.
"Avere un sistema immunitario debole", in realtà, non significa nulla da un punto di vista biologico. Se una persona si ammala di frequente, sviluppando influenze, riniti, rinofaringiti ricorrenti, ecc. non è a causa di un sistema immunitario debole, ma a causa di conflittualità recidivanti e/o di riparazioni in sospeso.
Se la persona è molto sensibile ai conflitti di distacco e separazione, per suoi vissuti passati, e continua a rimanere in relazioni altalenanti, non ha un sistema immunitario debole, ma una particolare resistenza a cambiare la propri vita e la propria percezione.
Se la persona è sempre sospettosa, impaurita e angosciata, vive in uno stato in cui basta poco per causare un conflitto di minaccia di territorio, spavento, paura frontale, paura nella nuca e via dicendo.
Il sistema immunitario può perdere la sua efficienza per l'azione costante e deleteria dell'ormone dello stress (cortisolo) e la stimolazione sintomatica del sistema immunitario non sortisce alcun effetto duraturo.
- Alimentazione: soprattutto quella sbrigativa, troppo raffinata e consumata senza amore
- Emozioni: paura, ansia, stress, tristezza, disgusto
- Sedentarietà o Attività forzate e non amate
Poi occorre andare all'origine della propria permeabilità percettiva e diatesi conflittuale. Lo si può fare cercando di esprimere emozioni soffocate, analizzando il rapporto con i genitori, il Progetto Senso e gli intrecci Transgenerazionali.
A cosa ci si immunizza con la malattia?
La malattia, ovvero la presenza di sintomi, deriva dalla soluzione di un conflitto biologico e rappresenta la fase di riparazione.
Il conflitto è stato risolto e la persona, il suo subconscio, ha probabilmente spinto in coscienza la ragione emotiva della conflittualità, rendendola impermeabile a quella conflittualità.
Nel contempo il sistema immunitario ha prodotto i suoi anticorpi e l'immunità umorale e cellulare per quel tipo di sentito biologico e per il tipo di microorganismo coinvolto in tale sentito e nei relativi tessuti attivati.
In buona sostanza si tratta di una immunità bio-emotivo-percettiva su almeno due livelli (emotivo e corporale) e permette all'individuo una evoluzione. Egli "ha imparato olisticamente" a non ricadere nello stesso conflitto.
A cosa ci si immunizza con la vaccinazione?
La vaccinazione toglie di mezzo l'importanza dell'esperienza conflittuale, stimolando il sistema immunitario in modo unicamente umorale e strutturale.
La persona è immune al microbo (anche e è noto che non tutte le persone si immunizzano con il vaccino) ma non al conflitto che, in fase di riparazione, richiede l'azione di quel microbo.
In altre parole "ha imparato solo il corpo", ma non l'intera persona proprietaria di quel corpo. Ha imparato il corpo, ma non la sua vita e il modo di viverla. È immune il corpo, ma non la persona.
Si tratta di una immunità incompleta, il che spiega la necessità dei richiami vaccinali, o le mancate immunizzazioni o le malattie intervenute anche dopo la vaccinazione.
Finché la Medicina Ufficiale non compirà studi approfonditi sul rapporto tra vissuto e fisiologia del sistema immunitario, la pratica della vaccinazione rimane una azione supponente, pericolosa e di fatto senza fondamenti scientifici e stabilità di risultati.



